با اشتراک در خبرنامه همیشه از آخرین تخفیفات و رویدادهای مهم ما مطلع خواهید شد

آمونیوم هپتامولیبدات (دکتر مجللی) Ammonium heptamolybdate
آمونیوم هپتامولیبدات تتراهیدرات (آمونیوم هپتا مولیبدات 4 آبه)
تضمین کیفیت و اصالت کالا
ارسال سریع به سراسر کشور
بازگشت کالا به دلیل "انصراف از خرید" در صورتی مورد قبول است که پلمپ کالا باز نشده باشد.
معرفی آمونیوم هپتامولیبدات
آمونیوم هپتامولیبدات (Ammonium heptamolybdate) با فرمول شیمیایی (NH4)6Mo7O24 یک ترکیب معدنی مهم است که کاربردهای فراوانی در صنایع مختلف دارد. این ماده به طور معمول به صورت تتراهیدرات (چهار آبه) یافت می شود که به صورت جامد بلوری سفید رنگ است که در آب به خوبی حل میشوند..یک ترکیب شیمیایی است که از مولیبدن و آمونیوم تشکیل شده است .
آمونیوم هپتامولیبدات معمولاً از واکنش محلولهای آمونیوم مولیبدات با اسید مولیبدیک یا با کاهش مولیبدن اکسید در حضور آمونیاک و حرارت تولید میشود. این فرآیند به دقت کنترل شده و به شرایط خاصی برای حفظ خلوص بالا نیاز دارد.
آمونیوم هپتامولیبدات بیشتر به عنوان یک معرف Reagent برای اندازه گیری میزان فسفات، سیلیکات، آرسنات و سرب در محلول های آبی استفاده می شود. (مانند آب رودخانه یا دریا). از آمونیوم هپتامولیبدات برای ساخت فلز خاکستری (مولیبدن) و یا سرامیک نیز استفاده می شود. می توان از آن به عنوان کاتالیزور در هیدروژن زدایی و یا گوگردزدایی نیز استفاده کرد.
تاریخچه کشف آمونیوم هپتامولیبدات
آمونیوم هپتامولیبدات، که در قالب ترکیبات مولیبدات مورد بررسی و استفاده قرار میگیرد، در تاریخچه شیمی دارای جایگاه مهمی است. اگرچه زمان دقیق کشف این ماده به خوبی مستند نشده است، ترکیبات مولیبدن به طور کلی از قرن ۱۸ میلادی شناخته شدهاند.
مولیبدن خود ابتدا توسط کارل ویلهلم شیله، یک شیمیدان سوئدی، در سال ۱۷۷۸ به عنوان یک عنصر جداگانه شناسایی شد. پیش از این، اغلب با سایر مواد معدنی مانند گرافیت یا سولفید سرب اشتباه گرفته میشد.
در طول قرن ۱۹ و اوایل قرن ۲۰، ترکیبات مختلفی از مولیبدن، از جمله آمونیوم مولیبدات و آمونیوم هپتامولیبدات، توسط شیمیدانان مختلف مورد بررسی قرار گرفتند. این ترکیبات به دلیل ویژگیهای شیمیایی منحصر به فردشان، به خصوص در واکنشهای اکسیداسیون و کاربردهای آزمایشگاهی، مورد توجه قرار گرفتند.
روش تولید آمونیوم هپتامولیبدات
دو روش اصلی برای تولید آمونیوم هپتامولیبدات (NH4)6Mo7O24·4H2O وجود دارد:
1. روش رسوب دهی:
این روش رایج ترین روش تولید آمونیوم هپتامولیبدات در مقیاس صنعتی است. مراحل کلی این روش به شرح زیر است:
- حل کردن تری اکسید مولیبدن (MoO3):
تری اکسید مولیبدن در آب داغ یا محلول آمونیاک رقیق حل می شود. - تنظیم pH
: pH محلول با استفاده از اسید یا باز به حدود 5 تا 6 تنظیم می شود. - رسوب دهی:
آمونیاک به محلول اضافه می شود تا زمانی که آمونیوم هپتامولیبدات به صورت رسوب سفید رنگ از محلول جدا شود. - فیلتراسیون و شستشو:
رسوب آمونیوم هپتامولیبدات فیلتر شده و با آب شسته می شود تا ناخالصی ها از بین بروند. - خشک کردن:
رسوب فیلتر شده در دمای کم (حدود 50 درجه سانتیگراد) خشک می شود تا پودر آمونیوم هپتامولیبدات به دست آید.
2.روش تبخیر:
این روش ساده تر از روش رسوب دهی است و معمولاً برای تولید مقادیر کم آمونیوم هپتامولیبدات در آزمایشگاه استفاده می شود. مراحل کلی این روش به شرح زیر است:
- حل کردن تری اکسید مولیبدن (MoO3):
تری اکسید مولیبدن در محلول آمونیاک آبی حل می شود. - تبخیر:
محلول در دمای اتاق تبخیر می شود تا زمانی که آمونیوم هپتامولیبدات به صورت کریستال های شش وجهی از محلول جدا شود. - جداسازی کریستال ها:
کریستال های آمونیوم هپتامولیبدات با فیلتر کردن از محلول جدا می شوند. - شستشو و خشک کردن:
کریستال ها با آب شسته می شوند و در دمای کم (حدود 50 درجه سانتیگراد) خشک می شوند.
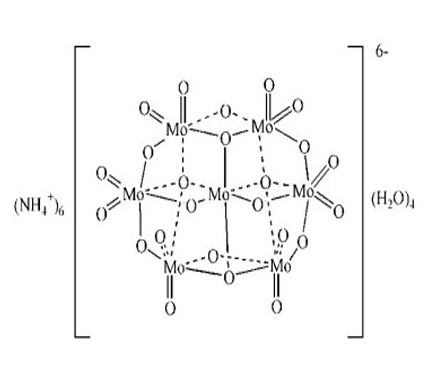
ساختار آمونیوم هپتامولیبدات
آمونیوم هپتامولیبدات (NH4)6Mo7O24·4H2O یک ترکیب معدنی با ساختار پیچیده است که از واحدهای اکتاهدرال [MoO6] تشکیل شده است. این واحدها به هم پیوسته اند و شبکه ای سه بعدی را تشکیل می دهند.
در مرکز هر اکتاهدر، یک اتم مولیبدن (Mo) قرار دارد که توسط شش اتم اکسیژن (O) احاطه شده است. این اتم های اکسیژن در گوشه های یک اکتاهدر قرار دارند و با پیوندهای کووالانسی به اتم مولیبدن متصل می شوند.
واحدهای اکتاهدرال [MoO6] از طریق گوشه های مشترک اکسیژن به هم متصل می شوند. این نوع اتصال منجر به تشکیل زنجیره ها، صفحات و ساختارهای سه بعدی پیچیده می شود.
یون های آمونیوم (NH4+) در حفره های موجود در ساختار شبکه سه بعدی آمونیوم هپتامولیبدات قرار می گیرند. این یون ها با پیوندهای هیدروژنی به اتم های اکسیژن متصل می شوند و به حفظ پایداری ساختار کمک می کنند.
چهار مولکول آب در ساختار آمونیوم هپتامولیبدات به صورت چهارآبه (چهار مولکول آب متصل به یک واحد) وجود دارد. این مولکول های آب نیز با پیوندهای هیدروژنی به اتم های اکسیژن متصل می شوند و به حفظ پایداری ساختار کمک می کنند.
جدول مشخصات آمونیوم هپتامولیبدات
مشخصه | مقدار | واحد |
نام شیمیایی | آمونیوم هپتامولیبدات | - |
فرمول شیمیایی | (NH4)6Mo7O24·4H2O | - |
جرم مولی | 1235.86 | گرم بر مول |
ظاهر | جامد بلوری سفید رنگ | - |
چگالی | 2.498 | گرم بر سانتی متر مکعب |
نقطه ذوب | 90 درجه سانتیگراد (از دست دادن آب)؛ 190 درجه سانتیگراد (تجزیه) | درجه سانتیگراد |
حلالیت در آب | 65.3 گرم در 100 میلی لیتر آب (تتراهیدرات) | گرم در 100 میلی لیتر |
pH محلول آبی | 5 تا 6 | - |
دمای نگهداری | 10 تا 25 درجه سانتیگراد | درجه سانتیگراد |
رطوبت نسبی نگهداری | 30 تا 50 درصد | درصد |
کاربردهای آمونیوم هپتامولیبدات
آمونیوم هپتامولیبدات (NH4)6Mo7O24·4H2O کاربردهای فراوانی در صنایع مختلف دارد، از جمله:
تولید فلز مولیبدن:
یکی از مهمترین کاربردهای آمونیوم هپتامولیبدات به عنوان ماده اولیه برای تولید فلز مولیبدن با استفاده از فرآیندهای مختلف مانند رسوب دهی و احیا است. مولیبدن فلزی با ارزش با کاربردهای فراوان در صنایع مختلف مانند فولادسازی، الکترونیک، هوافضا و پزشکی است.
سرامیک:
از آمونیوم هپتامولیبدات به عنوان یک افزودنی در تولید سرامیک های خاص برای افزایش استحکام و پایداری حرارتی استفاده می شود. این ماده به دلیل پایداری حرارتی بالا و خواص ضد حریق، در ساخت سرامیک های نسوز و دیرگداز نیز کاربرد دارد.
کود:
در برخی از کودها از آمونیوم هپتامولیبدات به عنوان منبع مولیبدن برای گیاهان استفاده می شود. مولیبدن یک عنصر ضروری برای رشد گیاهان است و نقش مهمی در تثبیت نیتروژن و سنتز اسیدهای آمینه ایفا می کند.
کاتالیزور:
از آمونیوم هپتامولیبدات به عنوان یک کاتالیزور فعال در کاتالیزورهای هیدروژن زدایی و گوگرد زدایی استفاده می شود. این ماده به دلیل فعالیت کاتالیزوری بالا و پایداری حرارتی، در تصفیه فرآورده های نفتی و گاز طبیعی کاربرد دارد.
رنگرزی:
در صنعت رنگرزی منسوجات از آمونیوم هپتامولیبدات به عنوان یک عامل تثبیت کننده رنگ استفاده می شود. این ماده به دلیل تمایل به اتصال به مولکول های رنگ، به تثبیت رنگ ها بر روی الیاف منسوجات کمک می کند.
آزمایشگاه:
در آزمایشگاه های شیمی از آمونیوم هپتامولیبدات به عنوان یک معرف تحلیلی برای اندازه گیری فسفات، سیلیکات، آرسنات و سرب در محلول های آبی استفاده می شود. این ماده به دلیل واکنش پذیری بالا و اختصاصیت به این ترکیبات، در روش های مختلف آنالیز شیمیایی کاربرد دارد.
کاربردهای دیگر:
علاوه بر موارد ذکر شده، از آمونیوم هپتامولیبدات در کاربردهای دیگری نیز استفاده می شود. مانند:
- تصفیه آب
- ساخت باتری
- تولید مواد ضد حریق
- داروسازی
خطرات آمونیوم هپتامولیبدات
آمونیوم هپتامولیبدات (NH4)6Mo7O24·4H2O در صورت بلعیدن، استنشاق یا جذب از طریق پوست می تواند سمی باشد. علائم مسمومیت با آمونیوم هپتامولیبدات شامل موارد زیر است:
- تهوع:
تهوع و استفراغ از جمله شایع ترین علائم مسمومیت با آمونیوم هپتامولیبدات هستند. - اسهال:
اسهال می تواند به دلیل تحریک دستگاه گوارش توسط آمونیوم هپتامولیبدات رخ دهد. - سرگیجه و سردرد:
سرگیجه و سردرد می تواند به دلیل اثر نوروتوکسیک آمونیوم هپتامولیبدات بر سیستم عصبی باشد. - ضعف و خستگی:
ضعف و خستگی می تواند به دلیل افت فشار خون یا سایر ناهنجاری های متابولیکی ناشی از مسمومیت با آمونیوم هپتامولیبدات باشد. - تشنج و کما:
در موارد شدید مسمومیت با آمونیوم هپتامولیبدات، تشنج و کما می تواند رخ دهد. - مرگ:
در موارد بسیار شدید مسمومیت با آمونیوم هپتامولیبدات، مرگ می تواند رخ دهد.
نحوه دفع آمونیوم هپتامولیبدات
دفع آمونیوم هپتامولیبدات (NH4)6Mo7O24·4H2O باید با احتیاط و مطابق با قوانین و مقررات محلی انجام شود. مراحل کلی دفع این ماده به شرح زیر است:
1. طبقه بندی:
اولین قدم در دفع آمونیوم هپتامولیبدات، طبقه بندی صحیح آن به عنوان یک ماده خطرناک است. این ماده به عنوان یک ماده سمی و خورنده طبقه بندی می شود و باید با احتیاط بیشتری با آن برخورد شود.
2. جداسازی:
آمونیوم هپتامولیبدات باید از سایر مواد زائد جدا شود. این کار برای جلوگیری از آلودگی سایر مواد و محیط زیست ضروری است.
3. بسته بندی:
آمونیوم هپتامولیبدات باید در ظروف مناسب و مهر و موم شده بسته بندی شود. این ظروف باید از موادی ساخته شده باشند که در برابر خوردگی توسط آمونیوم هپتامولیبدات مقاوم باشند.
4. برچسب گذاری:
ظروف حاوی آمونیوم هپتامولیبدات باید به درستی برچسب گذاری شوند. برچسب ها باید شامل اطلاعاتی در مورد محتوای ظرف، خطرات سلامتی و ایمنی و دستورالعمل های دفع باشد.
5. حمل و نقل:
آمونیوم هپتامولیبدات باید توسط افراد واجد شرایط و با استفاده از وسایل نقلیه مناسب حمل و نقل شود.
6. دفع نهایی:
روش های مختلفی برای دفع نهایی آمونیوم هپتامولیبدات وجود دارد، از جمله:
- محو سازی:
آمونیوم هپتامولیبدات با استفاده از حرارت بالا به اکسید مولیبدن (MoO3) و بخار آمونیاک (NH3) تبدیل می شود. - دفن:
آمونیوم هپتامولیبدات در محل های دفن زائدات خطرناک دفن می شود. - بازیافت:
از آمونیوم هپتامولیبدات می توان برای بازیافت مولیبدن استفاده کرد.
نگهداری و بستهبندی آمونیوم هپتامولیبدات
برای نگهداری و بستهبندی آمونیوم هپتامولیبدات، باید توجه به عواملی مانند حفظ خلوص ماده، جلوگیری از آلودگی، ایمنی کارگران و راهکارهای محیطی مناسب داشت. در زیر به برخی از نکات مهم در این زمینه اشاره میشود:
1. ظروف و شرایط ذخیرهسازی:
- آمونیوم هپتامولیبدات باید در ظروفی با غلظتهای مشخص و شرایط دمایی و رطوبتی مناسب نگهداری شود.
- این ماده باید در ظروفی با پوشش مناسب و از جنس مقاوم در برابر مواد شیمیایی و خوردگی قرار گیرد.
2. جلوگیری از آلودگی:
- برای جلوگیری از آلودگی، ظروف نگهداری و بستهبندی باید قبل از استفاده کاملاً تمیز شده و آزاد از هر گونه مواد آلوده باشند.
- هنگام انتقال آمونیوم هپتامولیبدات، باید از تماس با مواد آلوده و آلودگی ظروف جلوگیری شود.
3. برنامهریزی ایمنی:
- تأمین ایمنی کارگران از طریق آموزشهای مرتبط با نگهداری و بستهبندی مواد شیمیایی خطرناک مانند آمونیوم هپتامولیبدات.
- استفاده از تجهیزات ایمنی شخصی مانند دستکش، عینک و ماسک محافظ در هنگام کار با این ماده.
4. محیط زیست:
- اطمینان از اینکه هنگام دفع بستهبندیهای قابل بازیافت استفاده شده و درستی آنها از لحاظ محیط زیستی در نظر گرفته شده است.
- جلوگیری از ورود آمونیوم هپتامولیبدات به آبهای سطحی یا زیرزمینی تا جلوگیری از آلودگی محیط زیست.
با رعایت این نکات و استفاده از روشهای مناسب نگهداری و بستهبندی، میتوان از ایمنی کارکنان، حفظ خلوص ماده و کاهش تأثیرات محیطی ناشی از آمونیوم هپتامولیبدات اطمینان حاصل کرد.
فروش آمونیوم هپتامولیبدات
فروشگاه ای آز فعال در حوزه فروش اینترنتی مواد شیمیایی آزمایشگاهی و صنعتی و لوازم و تجهیزات آزمایشگاهی است که آماده فروش آمونیوم هپتامولیبدات در بسته بندی های مقرون به صرفه و با کیفیت ممتاز در گریدهای صنعتی و آزمایشگاهی و از برندهای معتبر ایرانی، هندی، چینی و اروپایی به پژوهشگران، دانشگاهیان، صنایع و کارخانجات است.
خرید آمونیوم هپتامولیبدات دکتر مجللی
کاربر موظف است پیش از اقدام به خرید این کالا، صفحه قوانین و مقررات وبسایت را مطالعه کند. جهت خرید آمونیوم هپتامولیبدات می توانید از بخش "افزودن به سبد خرید" اقدام به ثبت سفارش کالای مورد نظر در وبسایت کنید. از طریق پیامک، واتس اپ، ایتا و روبیکا با شماره 09925021003 نیز می توانید کالای مورد نظر را مستقیما از شرکت خریداری کنید.
آیا آمونیوم هپتامولیبدات موادی مضر برای سلامتی است؟
بله، آمونیوم هپتامولیبدات ممکن است موادی مضر برای سلامتی انسانها و محیط زیست باشد، به خصوص در صورت استفاده نادرست یا دفع نامناسب آن.
چگونه میتوانیم از آسیبهای آمونیوم هپتامولیبدات جلوگیری کنیم؟
برای جلوگیری از آسیبهای مرتبط با آمونیوم هپتامولیبدات، باید از ایمنی کارگران، استفاده از تجهیزات حفاظتی، نگهداری و بستهبندی مناسب، دفع به درستی و با رعایت قوانین و مقررات محلی و ملی اطمینان حاصل کرد.
آیا آمونیوم هپتامولیبدات میتواند به آبهای زیرزمینی یا سطحی نفوذ کند؟
بله، در صورت دفع نامناسب، آمونیوم هپتامولیبدات میتواند به آبهای زیرزمینی یا سطحی نفوذ کرده و باعث آلودگی آنها شود. بنابراین، باید از روشهای مناسب دفع و جلوگیری از نفوذ آن به آبها استفاده شود.
آیا آمونیوم هپتامولیبدات برای استفاده در محیطهای غذایی مناسب است؟
استفاده از آمونیوم هپتامولیبدات در محیطهای غذایی ممکن است منجر به آلودگی مواد غذایی شود. بنابراین، بهتر است از این ماده در محیطهایی که با مواد غذایی در ارتباط هستند، خودداری شود.
آیا آمونیوم هپتامولیبدات با فلزات واکنش دارد؟
بله، آمونیوم هپتامولیبدات میتواند با برخی از فلزات واکنش دهد و ترکیبات مختلفی ایجاد کند، به ویژه در حضور اسید یا باز و شرایط خاص.
آیا آمونیوم هپتامولیبدات در حضور نور مستقیم واکنش دارد؟
آمونیوم هپتامولیبدات در حضور نور مستقیم واکنش قابل توجهی ندارد و پایدار است. اما در شرایط بسیار سخت و شدید ممکن است تحت تأثیر نور مستقیم تجزیه شود.
 آمونیوم هپتامولیبدات (دکتر مجللی)
آمونیوم هپتامولیبدات (دکتر مجللی)