با اشتراک در خبرنامه همیشه از آخرین تخفیفات و رویدادهای مهم ما مطلع خواهید شد

سدیم هیدروژن کربنات (قطران شیمی) Sodium bicarbonate
مناسب مدارس و اهداف آموزشی
مناسب کارهای آزمایشگاهی، کارگاهی، صنایع و کارخانجات
خریدار موظف است کلیه دستورالعمل های استعمال مربوطه را مطالعه و با اطلاع کافی آن را خریداری کند.
پوشیدن دستکش، ماسک و عینک آزمایشگاهی الزامیست.
از بلیعدن، تماس با پوست و استنشاق خودداری کنید.
ارسال به سراسر کشور
متاسفانه این کالا در حال حاضر موجود نیست.
بازگشت کالا به دلیل "انصراف از خرید" در صورتی مورد قبول است که پلمپ کالا باز نشده باشد.
معرفی سدیم هیدروژن کربنات
بی کربنات سدیم (NaHCO3) که به آن جوش شیرین، بی کربنات سودا یا سدیم هیدروژن کربنات نیز می گویند، جامد کریستالی یا پودری سفید رنگ است که منبع دی اکسید کربن است و به عنوان یک ماده در بکینگ پودرها، نمک های جوشان و نوشیدنی ها استفاده می شود. به عنوان جزئی از کپسول های آتش نشانی خشک شیمیایی. قلیایی بودن خفیف آن آن را برای درمان اسیدیته معده یا ادرار و اسیدوز مفید می کند. همچنین در فرآیندهای صنعتی خاصی مانند دباغی و تهیه پشم استفاده می شود. بی کربنات سدیم به صورت صنعتی از کربنات سدیم تولید می شود.
بسیاری از محصولات نانوایی توسط دی اکسید کربن حاصل از اضافه کردن جوش شیرین یا بی کربنات سدیم در بکینگ پودر خمیر می شوند. بی کربنات سدیم در فرآیندی برای از بین بردن رنگ و خوردگی به نام سودابلاست استفاده می شود. به عنوان یک محیط انفجار، بی کربنات سدیم برای حذف آلودگی های سطحی از بسترهای نرم تر و کم ارتجاعی مانند آلومینیوم، مس یا الوار که ممکن است توسط رسانه های ساینده شن سیلیس آسیب ببینند، استفاده می شود. بی کربنات سدیم به عنوان مکمل خوراک گاو، به ویژه به عنوان یک عامل بافر برای شکمبه استفاده می شود. بی کربنات سدیم مخلوط با آب می تواند به عنوان یک ضد اسید برای درمان سوء هاضمه اسیدی و سوزش سر دل استفاده شود. بی کربنات سدیم زمانی که روی برگ ها استفاده شود، می تواند از رشد قارچ ها جلوگیری کند. با این حال، قارچ را از بین نمی برد. مقدار بیش از حد سدیم هیدروژن کربنات می تواند باعث تغییر رنگ میوه ها (محلول دو درصد) و کلروز (محلول یک درصد) شود. بی کربنات سدیم را می توان برای خاموش کردن چربی های کوچک یا آتش های الکتریکی با انداختن روی آتش استفاده کرد، زیرا گرم شدن بی کربنات سدیم باعث آزاد شدن دی اکسید کربن می شود.
ویژگی های سدیم هیدروژن کربنات
بی کربنات سدیم یک ترکیب آمفوتریک است. محلول های آبی به دلیل تشکیل اسید کربنیک و یون هیدروکسید کمی قلیایی هستند. سدیم هیدروژن کربنات اغلب می تواند به عنوان جایگزین ایمن تری برای هیدروکسید سدیم استفاده شود و به همین دلیل می توان از آن به عنوان شستشو برای حذف هرگونه ناخالصی اسیدی از مایع "خام" استفاده کرد و نمونه خالص تری تولید کرد. از واکنش بی کربنات سدیم و اسید، نمک و اسید کربنیک تولید می شود که به آسانی به دی اکسید کربن و آب تجزیه می شود. در دمای 80 تا 100 درجه سانتیگراد (176 تا 212 درجه فارنهایت)، بی کربنات سدیم به تدریج به کربنات سدیم، آب و دی اکسید کربن تجزیه می شود. ساختار شیمیایی سدیم هیدروژن کربنات در شکل زیر ارائه شده است:
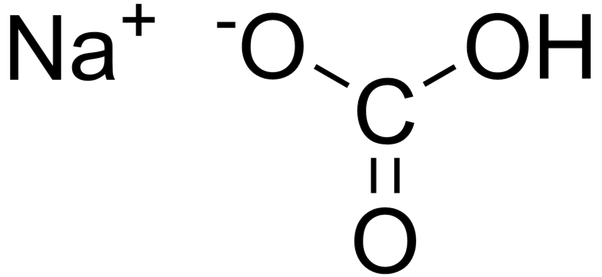
کاربرد سدیم هیدروژن کربنات
- صنعت نساجی
- تولید پلاستیک و پلیمرهای پیچیده
- ضدعفونی کردن میوه ها و سبزیجات و آشپزخانه
- برق انداختن ظروف نقره
- تصفیه هوا
- دئودورانت
- به عنوان دهانشویه
- افزایش حجم خمیر
- محصولات مراقبت شخصی و داروها
- شوینده ها و حلال ها
- سفید کنندگی و تمیز کنندگی پارچه در خشک شویی ها
کاربرد سدیم هیدروژن کربنات قطران شیمی
- مناسب برای مدارس (اهداف آموزشی)
- مناسب دانشگاه ها و مراکز تحقیقاتی
- مناسب صنایع و کارخانجات
- مناسب صنایع خانگی و کارگاهی
فروش سدیم هیدروژن کربنات قطران شیمی
فروشگاه ای آز فعال در حوزه فروش اینترنتی مواد شیمیایی آزمایشگاهی و صنعتی و لوازم و تجهیزات آزمایشگاهی است که آماده فروش سدیم هیدروژن کربنات در بسته بندی های مقرون به صرفه و با کیفیت ممتاز در گرید آموزشی و آزمایشگاهی و از برندهای معتبر ایرانی، هندی، چینی و اروپایی به مدارس، دانشگاه ها، مراکز تحقیقاتی، صنایع و کارخانجات است.
خرید سدیم هیدروژن کربنات قطران شیمی
کاربر موظف است پیش از اقدام به خرید این کالا، صفحه قوانین و مقررات وبسایت را مطالعه کند. جهت خرید سدیم هیدروژن کربنات می توانید از بخش "افزودن به سبد خرید" اقدام به ثبت سفارش کالای مورد نظر در وبسایت کنید. از طریق واتس اپ، ایتا، روبیکا با شماره 09925021003 نیز می توانید کالای مورد نظر را مستقیما از شرکت خریداری کنید.
 سدیم هیدروژن کربنات (قطران شیمی)
سدیم هیدروژن کربنات (قطران شیمی)
متاسفانه این کالا در حال حاضر موجود نیست.





















