با اشتراک در خبرنامه همیشه از آخرین تخفیفات و رویدادهای مهم ما مطلع خواهید شد

متانول (دکتر مجللی) Methanol (Extra pure)
تضمین اصالت کالا
ارسال به سراسر کشور
بازگشت کالا به دلیل "انصراف از خرید" در صورتی مورد قبول است که پلمپ کالا باز نشده باشد.
معرفی متانول آزمایشگاهی
متانول که در میان نامهای دیگر با نام متیل الکل نیز شناخته میشود، یک ماده شیمیایی آلی و سادهترین الکل با فرمول CH3OH (گروه متیل مرتبط با گروه هیدروکسیل، اغلب به اختصار MeOH) است. این یک مایع سبک، فرار، بی رنگ و قابل اشتعال با بوی الکلی متمایز مشابه بوی اتانول (الکل قابل شرب) است. متانول یک حلال قطبی نام الکل چوب را به خود اختصاص داد زیرا زمانی عمدتاً از تقطیر مخرب چوب تولید می شد. امروزه متانول عمدتاً به صورت صنعتی با هیدروژنه کردن مونوکسید کربن تولید می شود.
متانول به عنوان یک مایع نسبتاً فرار بی رنگ با بوی تند کمی شیرین مانند الکل اتیلیک به نظر می رسد. کاملا با آب مخلوط می شود. بخارها کمی سنگین تر از هوا هستند و ممکن است مقداری مسافت را تا منبع احتراق طی کنند و به عقب برگردند. هر گونه انباشته شدن بخار در فضاهای محدود، مانند ساختمان ها یا فاضلاب، ممکن است در صورت مشتعل شدن منفجر شود. برای ساخت مواد شیمیایی، برای حذف آب از سوخت های خودرو و هواپیما، به عنوان حلال رنگ ها و پلاستیک ها، و به عنوان یک عنصر در طیف گسترده ای از محصولات استفاده می شود.

تاریخچه و پیشینه کشف متانول
متانول، یکی از مهمترین الکلها در صنعت شیمیایی، به صورت اولیه از چوب تولید میشد. اولین بار متانول به عنوان یک ماده شیمیایی توسط روبرت بویل در سال ۱۶۶۱ با نام "spirit of wood" (روح چوب) شناخته شد. اما فرآیند تصفیه و استخراج متانول به صورت خالص اولین بار در قرن نوزدهم توسط سایمون لیون کوهلر انجام شد. سپس، در دهه ۱۹۲۰، فرآیند هیدروژنولیز گاز سنتزی برای تولید متانول توسط بایر بهبود یافت و تبدیل به یکی از روشهای اصلی تولید متانول شد. از آن زمان به بعد، فناوریهای جدیدی برای تولید متانول توسعه یافته و این الکل یکی از مواد اصلی و حیاتی در صنایع شیمیایی و سوختهای تجدیدپذیر شد.
ساختار متانول
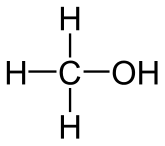
متانول یا الکل متیلیک (CH3OH) دارای ساختار شیمیایی سادهای است. در این مولکول، یک اتم کربن به سه اتم هیدروژن متصل است که از طریق یک اتصال اسیل به یک اتم اکسیژن به اتم کربن متصل میشود. ساختار متانول به صورت خطی است و این مولکول دارای یک گروه هیدروکسیل (-OH) است که به اتم کربن متصل است. به طور کلی، ساختار متانول به صورت زیر است:
روشهای تولید متانول
متانول، یکی از مهمترین مواد اولیه در صنعت شیمیایی است و از متغیرهای بسیاری برای تولید آن استفاده میشود. در زیر، روشهای متداول تولید متانول آورده شده است:
- تبدیل گاز طبیعی (متان) به متانول:
این روش شامل فرآیند کاتالیزوری است که متان (CH4) از گاز طبیعی با اکسیژن (O2) تحت شرایط دما و فشار مناسب با استفاده از کاتالیزورهایی مانند مس-مولیبدن یا کبالت-زینک به متانول (CH3OH) تبدیل میشود. - فرآیند هیدروژنولیز گاز سنتزی:
در این فرآیند، گاز سنتزی که شامل دیاکسید کربن (CO) و هیدروژن (H2) است، تحت شرایط کاتالیزوری و با استفاده از کاتالیزورهایی مانند آلومینا یا فریت، به متانول تبدیل میشود. - تبدیل گاز زغالسنگ به متانول:
در این فرآیند، گاز سنتزی از زغالسنگ با استفاده از فرآیند گاز سازی، تحت شرایط کاتالیزوری به متانول تبدیل میشود. - تبدیل بیوماس به متانول:
این روش شامل تبدیل بیوماس مانند چوب، پوست و پوسته میوهها و مواد آلی دیگر به گاز (گاز سنتزی) و سپس تبدیل آن به متانول میشود.
این روشها فقط چند نمونه از روشهای تولید متانول هستند و هر کدام ممکن است با توجه به شرایط محلی و اقتصادی، در صنایع مختلف مورد استفاده قرار گیرند.
جدول مشخصات و ویژگیهای متانول
| مشخصه | مقدار |
| فرمول شیمیایی | CH3OH |
| نام دیگر | الکل متیلیک |
| وزن مولکولی | 32.04 گرم/مول |
| شکل و حالت فیزیکی | مایع بیرنگ و بیبو |
| دمای ذوب | -97.6 درجه سانتیگراد |
| دمای جوش | 64.7 درجه سانتیگراد |
| چگالی | 0.7918 گرم/سانتیمتر مکعب |
| حلالیت در آب | کاملاً حل شدن |
| نقطه اشتعال | 11 درجه سانتیگراد |
| دمای اشتعال | ۴۷۶ درجه سانتیگراد |
| حرارت انتشار مخصوص | 89.5 جول بر گرم.کل |
| ضریب شکست | 1.329 |
| ویسکوزیته | 0.5908 میلیپاسکالثانیه (در 20 درجه سانتیگراد) |
کاربردهای متانول آزمایشگاهی
متانول به عنوان یکی از مواد اولیه مهم در آزمایشگاهها مورد استفاده قرار میگیرد و در بسیاری از فعالیتهای آزمایشگاهی به دلایل مختلف مورد استفاده قرار میگیرد. برخی از کاربردهای متداول آن در آزمایشگاهها عبارتند از:
- محلولپذیری و حلال:
متانول به عنوان یک حلال گسترده در آزمایشگاهها استفاده میشود، به خصوص در تهیه محلولهای مختلف و حلال کردن مواد آلی و غیرآلی. - خشککننده:
متانول به عنوان یک خشککننده در بسیاری از فرآیندهای آزمایشگاهی مورد استفاده قرار میگیرد، مانند خشک کردن گازها و حذف رطوبت از مواد. - تولید استانداردها و محلولهای استاندارد:
متانول برای تهیه محلولهای استاندارد و تهیه استانداردهای مربوط به تجزیه و تحلیل شیمیایی مورد استفاده قرار میگیرد. - فرآیندهای تصفیه:
در فرآیندهای تصفیه و پالایش مواد شیمیایی، متانول به عنوان یک ماده مهم جهت انجام فرآیندهای تصفیه و استخراج مواد مورد استفاده است. - آزمونهای آزمایشگاهی:
متانول برای انجام آزمونهای مختلف در آزمایشگاهها مورد استفاده قرار میگیرد، مانند تستهای آلودگی، تستهای اکسیداسیون و تجزیه و تحلیل مواد. - سنتز شیمیایی:
متانول به عنوان یک منبع کربن و هیدروژن در سنتزهای شیمیایی مختلف استفاده میشود. - خنک کننده:
در برخی از آزمایشها و فرآیندهای شیمیایی، متانول به عنوان یک ماده خنک کننده مورد استفاده قرار میگیرد. - محافظت از نمونهها:
متانول برای حفظ نمونهها و پیشگیری از رشد میکروارگانیسمها و پوسیدگی در آزمایشگاهها مورد استفاده قرار میگیرد.
این تنها برخی از کاربردهای متانول در آزمایشگاهها میباشد و در طی روند آزمایشی، ممکن است کاربردهای دیگری نیز برای آن پیدا شود.
متانول آزمایشگاهی شامل یک گروه متیل است که به یک گروه هیدروکسیل قطبی مرتبط است. با بیش از 20 میلیون تن تولید سالانه، به عنوان پیش ساز سایر مواد شیمیایی از جمله فرمالدئید، اسید استیک، متیل ترت بوتیل اتر، متیل بنزوات، آنیزول، پراکسی اسیدها و همچنین مجموعه ای از مواد شیمیایی تخصصی تر استفاده می شود. متانول در درجه اول به فرمالدئید تبدیل می شود که به طور گسترده در بسیاری از زمینه ها به ویژه پلیمرها استفاده می شود. این تبدیل مستلزم اکسیداسیون است.
متانول به عنوان یک دناتورانت برای اتانول استفاده می شود، این محصول به عنوان "الکل دناتوره" یا "روح متیله" شناخته می شود. این معمولاً در دوران ممنوعیت برای جلوگیری از مصرف مشروبات الکلی غیرقابل استفاده مورد استفاده قرار می گرفت و در نهایت منجر به مرگ چندین نفر شد. این نوع اعمال در حال حاضر در ایالات متحده غیرقانونی است و قتل تلقی می شود.
متانول به عنوان حلال و به عنوان ضد یخ در خطوط لوله و مایع شستشوی شیشه جلو استفاده می شود. متانول به عنوان ضدیخ خنک کننده خودرو در اوایل دهه 1900 مورد استفاده قرار گرفت. از می 2018، متانول در اتحادیه اروپا برای استفاده در شستشو یا یخ زدایی شیشه جلو به دلیل خطر مصرف انسانی آن ممنوع شد، در نتیجه مسمومیتهای متانول در جمهوری چک در سال 2012. در برخی از تصفیه خانههای فاضلاب، مقدار کمی متانول به فاضلاب اضافه میشود تا منبع غذایی کربنی برای باکتریهای نیتروژنکننده باشد که نیتراتها را به گاز نیتروژن تبدیل میکند و نیتریفیکاسیون سفرههای آب حساس را کاهش میدهد. متانول به عنوان یک عامل بی رنگ کننده در الکتروفورز ژل پلی آکریل آمید استفاده می شود.
دفع ضایعات متانول
دفع ضایعات متانول میتواند به دلایل مختلفی انجام شود، اما باید از روشی استفاده شود که هیچ تأثیر آسیبرسانی به محیط زیست و افرادی که در معرض قرار میگیرند، ایجاد نشود. برخی از روشهای متداول برای دفع ضایعات متانول عبارتند از:
- تصفیه و پالایش:
ضایعات متانول میتوانند تحت فرآیندهای تصفیه و پالایش شیمیایی قرار گیرند تا از مواد آلاینده و مضر جدا شوند و به حالتی مناسب برای دفع درآیند. - احتراق:
متداولترین روش برای دفع ضایعات متانول، احتراق آن در دستگاههای احتراقی است. این روش منجر به تبدیل متانول به دیاکسید کربن و آب میشود که اثرات زیست محیطی کمتری دارد. - منابع دیگر:
ضایعات متانول میتوانند در صورت امکان، بازیافت و استفاده مجدد شوند. این کار به حفظ منابع و کاهش زباله کمک میکند. - دیگر روشها:
بسته به شرایط محلی و مقررات محیط زیستی، ممکن است روشهای دیگری مانند استفاده از فرآیندهای بیولوژیکی یا استفاده از سیستمهای تصفیه آب و فاضلاب برای دفع ضایعات متانول مورد استفاده قرار گیرد.
نگهداری و بستهبندی متانول آزمایشگاهی
نگهداری و بستهبندی متانول آزمایشگاهی باید با دقت و به کمک استانداردهای ایمنی و مقررات محلی انجام شود. در زیر توصیههایی برای نگهداری و بستهبندی متانول آزمایشگاهی آورده شده است:
- ظروف محکم و مقاوم:
برای نگهداری متانول آزمایشگاهی از ظروف محکم و مقاوم در برابر تغییرات دما و فشار استفاده کنید. بهتر است از بطریهای شیشهای یا پلاستیکی با درپوش مناسب استفاده شود. - علامتگذاری مناسب:
همواره بطریها را با نام متانول علامتگذاری کنید و از آنها به عنوان یک ماده قابل اشتعال و سمی اطلاع دهید. همچنین، تاریخ تولید و انقضا را نیز روی بطریها نوشته و آنها را در محلی مخصوص و دور از دسترس کودکان نگهداری کنید. - محافظت از نور و حرارت:
متانول باید در محیط خنک و خشک و دور از نور مستقیم آفتاب نگهداری شود. همچنین از قرار گرفتن آن در معرض حرارت و آتش باید پرهیز شود. - استفاده از تجهیزات ایمنی:
همواره در هنگام برداشتن و استفاده از متانول، از تجهیزات ایمنی مانند عینک ایمنی، دستکش و ماسک استفاده کنید. همچنین در محل کار و نگهداری از متانول، آتشنشانی و تجهیزات خاموشکننده آتش قرار دهید. - تهویه مناسب:
محیطی با تهویه مناسب برای نگهداری متانول بسیار حیاتی است. اطمینان حاصل کنید که در محل نگهداری از متانول، تهویه و تهویه مناسب وجود دارد تا هرگونه تجمع بخارات متانول جلوگیری شود.
خطرات شیمیایی متانول
به شدت با اکسیدان های قوی مانند نیترات جیوه و یا پرکلریت منیزم واکنش داده و منجر به آتش سوزی و انفجار می شود. بین متانول و فلزاتی از قبیل پتاسیم، منیزیم، اکسیدکننده هایی مثل پرکلرات باریم، برومین کلرین، پراکسید هیدروژن و سدیم در صورت وجود حرارت خاصیت انفجاری ایجاد می شود. متانول با کلروفرم، دی اتیل روی، کلریدسیانوریک و نیتریک اسید شدیداً واکنش می دهد. درصورت تجزیه حرارتی به دی اکسیدکربن و فرمالدئید تولید می شود. متانول بسیار قابل اشتعال است. بخارات آن کمی سنگین تر از هوا است، می تواند حرکت کند و مشتعل شود. آتش سوزی متانول باید با مواد شیمیایی خشک، دی اکسید کربن، اسپری آب یا فوم مقاوم در برابر الکل خاموش شود.
اثرات مواجهه کوتاه مدت
- تحریک چشم ها
- تحریک دستگاه تنفسی
- تاثیر بر دستگاه اعصاب مرکزی
اثرات مواجهه طولانی مدت
- سبب تخریب چربی پوست
- تاثیر بر دستگاه تنفسی فوقانی و دستگاه اعصاب مرکزی و منجر به تحریک، سر درد، خستگی و فقدان تمرکز می شود.
- مصرف گوارشی آن منجر به سیروز کبدی می شود.
فروش متانول آزمایشگاهی دکتر مجللی

خرید متانول آزمایشگاهی دکتر مجللی
چه مقدار از متانول ایجاد سمیت می کند؟
مصرف کمتر از 10 میلی لیتر متانول خالص می تواند با تخریب عصب بینایی باعث کوری دائمی شود. 30 میلی لیتر (1.0 اونس آمریکا) به طور بالقوه کشنده است. متوسط دوز کشنده 100 میلی لیتر (3.4 اونس آمریکا)، یعنی 1-2 میلی لیتر بر کیلوگرم وزن بدن متانول خالص است. دوز مرجع برای متانول 0.5 میلی گرم بر کیلوگرم در روز است. اثرات سمی ساعت ها پس از مصرف شروع می شود و پادزهرها اغلب می توانند از آسیب دائمی جلوگیری کنند. به دلیل شباهتهای ظاهری و بو آن به اتانول (الکل موجود در نوشیدنیها)، تمایز بین این دو دشوار است. در مورد الکل دناتوره شده، مشروبات الکلی تقلبی یا نوشیدنی های الکلی با کیفیت بسیار پایین نیز چنین است.
متانول به چه دلیل به عنوان پیش ماده در تولید فرمالدئید استفاده میشود؟
متانول به عنوان پیش ماده در تولید فرمالدئید به دلیل واکنش اکسیداسیون با هوا به فرمالدئید که یک ماده مهم در صنایع پلاستیکی و رزینهاست، مورد استفاده قرار میگیرد.
آیا متانول میتواند به عنوان یک دناتورانت برای اتانول استفاده شود؟
بله، متانول به عنوان یک دناتورانت برای اتانول استفاده میشود و به عنوان "الکل دناتوره" یا "روح متیله" شناخته میشود.
آیا مصرف متانول به عنوان یک ماده خنککننده در صنعت خودروسازی با محیط زیست همخوانی دارد؟
مصرف متانول به عنوان ماده خنککننده در صنعت خودروسازی به دلیل خطرات زیست محیطی که به ویژه در صورت نشت میتواند ایجاد کند، با محیط زیست همخوانی ندارد. متانول باعث آلودگی آب و خطرات برای ارگانیسمهای زنده میشود، بنابراین استفاده از آن به عنوان یک ماده خنککننده ممنوع است.
آیا متانول تنها در تصفیه آب به عنوان منبع کربنی مورد استفاده قرار میگیرد؟
خیر، متانول علاوه بر استفاده در تصفیه آب به عنوان منبع کربنی، در صنایع مختلف از جمله صنایع پلاستیک، شیشهسازی، خودروسازی و آزمایشگاهها نیز مورد استفاده قرار میگیرد.
 متانول (دکتر مجللی)
متانول (دکتر مجللی)