با اشتراک در خبرنامه همیشه از آخرین تخفیفات و رویدادهای مهم ما مطلع خواهید شد
اسید هیدروکلریک 37% (اسید کلریدریک) (دکتر مجللی) Hydrochloric Acid (Extra pure)
این کالا با تضمین اصالت ارائه می گردد.
بطری پلاستیکی
نام های مترادف: جوهر نمک، اسید کلریدریک
بازگشت کالا به دلیل "انصراف از خرید" در صورتی مورد قبول است که پلمپ کالا باز نشده باشد.
معرفی اسید هیدروکلریک37% (دکتر مجللی)
از بین شش اسید معروف قوی از اسیدهای معدنی در شیمی، اسید هیدروکلریک ، یک پروتون دارد و کمترین تمایل را به شرکت در یک واکنش اکسایش-کاهش دارد. برخلاف اسیدی بودن آن، یکی از کم خطرترین اسیدها برای استفاده است زیرا شامل یون کلرید واکنش ناپذیر و غیر سمی است. محلولهای نسبتاً قوی اسید هیدروکلریک آزمایشگاهی در طول زمان نگهداری، کاملاً پایدار هستند و غلظت آنها در زمان ثابت میماند. این ویژگیها به علاوه این که به عنوان یک واکنشگر ناب خالص در دسترس است، اسید هیدروکلریک را به یک واکنش گر اسیدی عالی مبدل میسازد. استفاده از این اسید در استخراج طلا از بردهای الکترونیکی بسیار رایج شده است.
تاریخچه اسید هیدروکلریک
اسید هیدروکلریک، با فرمول شیمیایی HCl، یک اسید معدنی قوی است که از واکنش کلرید سدیم (NaCl) با اسید سولفوریک (H2SO4) تولید میشود. هیدروکلریک اسید برای اولین بار در قرن 13 میلادی توسط جابر بن حیان، دانشمند عرب، کشف شد. او این اسید را با حرارت دادن نمک در اسید نیتریک تولید کرد.
در قرن 16 میلادی، آندریاس لیباویوس، شیمیدان آلمانی، اسید هیدروکلریک را با حرارت دادن نمک در بوته چینی خاک رسی تولید کرد. این روش تولید هیدروکلریک اسید هنوز هم مورد استفاده قرار میگیرد.
در قرن 19 میلادی، با توسعه صنعت تولید فولاد، تقاضا برای اسید هیدروکلریک افزایش یافت. این اسید برای تولید کلرید آهن، که در تولید فولاد استفاده میشود، مورد نیاز است.
در حال حاضر،هیدروکلریک اسید یکی از پرکاربردترین اسیدهای صنعتی است. این اسید در صنایع مختلفی، از جمله تولید فولاد، پالایش نفت، تصفیه آب و فاضلاب، تولید کاغذ، تولید مواد شیمیایی و صنایع غذایی استفاده میشود.
جدول مشخصات فنی اسید هیدروکلریک
| فرمول مولکولی | HCl |
| جرم مولی | 36.46 g/mol |
| شکل ظاهری | مایع شفاف و بیرنگ تا زرد روشن |
| چگالی | 1.18 g/cm3 |
| انحلال پذیری در آب | کاملا محلول |
| نقطه ذوب | -85.05 °C |
نامهای متداول اسید هیدروکلریک
اسید هیدروکلریک با نامهای مختلفی شناخته میشود که برخی از آنها عبارتند از:
جوهر نمک
اسید کلریدریک
هیدروژن کلرید
کلرید هیدروژن
کاربرد اسید هیدروکلریک
تهیه تیزاب سلطانی
اسیدشویی فولاد
تولید ترکیبات آلی و شیمیایی
صنایع غذایی به عنوان کنترل کننده pH و خنثی سازی
بازسازی مبدل های یونی
چرم سازی
صنایع ساختمانی
اسید زنی چاه نفت
ساختار مولکولی اسید هیدروکلریک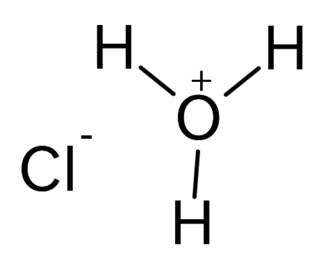
روشهای تولید اسید هیدروکلریک
روشهای مختلفی برای تولید هیدروکلریک اسید وجود دارد که برخی از آنها عبارتند از:
- روش کلر-آلکالی:این روش متداولترین روش تولید هیدروکلریک اسید است. در این روش، کلر و هیدروکسید سدیم با یکدیگر واکنش میدهند و اسید هیدروکلریک و هیدروکسید کلر تولید میکنند.
- روش نمک-سولفوریک:در این روش، نمک و اسید سولفوریک با یکدیگر واکنش میدهند و هیدروکلریک اسید و سولفات سدیم تولید میکنند.
- روش تبادل یونی:در این روش، نمک از طریق تبادل یونی با یک رزین تبادل یونی به هیدروکلریک اسید تبدیل میشود.
روش تولید هیدروکلریک اسید به عوامل مختلفی، از جمله میزان تولید، کیفیت اسید مورد نیاز و هزینه تولید، بستگی دارد.
مزایای اسید هیدروکلریک
- پایدار است و غلظت خود را در طول زمان حفظ می کند.
- تمایل کمتری به شرکت در واکنش اکسایش کاهش دارد.
- ویژگی جرم گیری و ضد عفونی کنندگی
- محلول در آب
دفع ضایعات اسید هیدروکلریک آزمایشگاهی
خطرات شیمیایی اسید هیدروکلریک

اثرات مواجهه کوتاه مدت اسید هیدروکلریک
- تحریک چشم هاوسوختگی وتخریب قرنیه چشم
- سوزش وسوختگی شدید پوستی
- احساس خفگی وگرفتگی صدا
اثرات مواجهه طولانی مدت اسید هیدروکلریک
- کبد را بشدت تحت تاثیر قرار می دهد.
- ایجاد التهاب وسوزش شدید در دستگاه گوارشی
- ایجاد اختلال در سیستم قلبی وعروقی
انبار و جابجایی اسید هیدروکلریک
هیدروکلریک اسید یک ماده شیمیایی خطرناک است که باید با احتیاط فراوان انبار شود.اسید هیدروکلریک باید در ظروف محکم و دربسته، ترجیحاً از جنس فلز ضد زنگ، انبار شود. این ظروف باید به طور ایمن برچسب گذاری شوند تا خطرات این اسید مشخص شود.
هیدروکلریک اسید باید در مکانی خشک و خنک انبار شود. این ماده باید دور از مواد قابل اشتعال و مواد اکسید کننده نگهداری شود.
اسید هیدروکلریک باید با احتیاط فراوان جابجا شود. هنگام جابجایی اسید هیدروکلریک، از تجهیزات ایمنی مناسب، مانند دستکش، عینک ایمنی، و ماسک، استفاده کنید.
نکات ایمنی و شرایط استفاده از اسید هیدروکلریک
اسید هیدروکلریک یک اسید قوی است که می تواند باعث سوختگی پوست، چشم، و دستگاه تنفسی شود. بنابراین، هنگام استفاده از اسید هیدروکلریک، باید نکات ایمنی زیر را رعایت کنید:
- از تماس اسید هیدروکلریک با پوست، چشم، و دستگاه تنفسی خودداری کنید.
- در صورت تماس هیدروکلریک اسید با پوست، بلافاصله محل تماس را با آب فراوان بشویید.
- در صورت تماس این اسید با چشم، بلافاصله چشم ها را با آب فراوان بشویید و پلک ها را به مدت 15 دقیقه باز نگه دارید.
- در صورت استنشاق هیدروکلریک اسید، بلافاصله هوای تازه استنشاق کنید و به پزشک مراجعه کنید.
- از تجهیزات ایمنی مناسب، مانند دستکش، عینک ایمنی، و ماسک، استفاده کنید.
- هیدروکلریک اسید را در ظروف محکم و دربسته نگهداری کنید.
- اسید هیدروکلریک را دور از دسترس کودکان و حیوانات خانگی قرار دهید.
بازار جهانی اسید هیدروکلریک
حجم بازار جهانی هیدروکلریک اسید در سال 2023، حدود 24.6 میلیارد دلار بوده است. این بازار انتظار می رود تا سال 2028، با نرخ رشد سالانه ترکیبی (CAGR) 4.5 درصد، به 32.4 میلیارد دلار برسد.
چین، ایالات متحده، و هند، سه کشور پیشرو در تولید هیدروکلریک اسید در جهان هستند. این سه کشور در مجموع، حدود 60 درصد از تولید جهانی این اسید را به خود اختصاص می دهند.
چین، ایالات متحده، و ژاپن، سه کشور پیشرو در مصرف هیدروکلریک اسید در جهان هستند. این سه کشور در مجموع، حدود 50 درصد از مصرف جهانی این اسید را به خود اختصاص می دهند
انتظار می رود بازار جهانی این اسید در سال های آینده، با نرخ رشد مناسبی رشد کند. این رشد به دلیل عوامل مختلفی، مانند افزایش تقاضا از صنایع مختلف، و توسعه فناوری های جدید، پیش بینی می شود.
فروش اسید هیدروکلریک آزمایشگاهی37%(دکتر مجللی)
خرید اسید هیدروکلریک آزمایشگاهی37%(دکتر مجللی)
آیا اسید هیدروکلریک همان تیزاب سلطانی است؟
تیزاب سلطانی محلولی بسیار خورنده است که همه فلزات حتی طلا را حل می کند و از ترکیب اسید هیدروکلریک و اسید نیتریک با نسبت حجمی 3 به 1 به دست می آید.
جوهر نمک چیست؟
جوهر نمک نام دیگر اسید هیدروکلریک یا همان اسید کلریدریک است.
آیا اسید هیدروکلریک غلیظ تر از 38% موجود است؟
به علت سرعت تبخیر بالا، غلظت های بالاتر از 40% از اسید کلریدریک از نظر شیمیایی پایدار نیست. بنابراین باید در نگهداری آن دقت شود چون در دما و فشار بالا، به غلظت های کمتر از 34% تنزل پیدا می کند.
آیا اسید هیدروکلریک سمی است؟
اسید هیدروکلریک تولید مه های اسیدی می کند که به شدت خورنده است و باعث آسیب های جدی به پوست، چشم، دستگاه گوارش و ریه می شود. باید هنگام کار با آن دستکش ضد اسید، عینک و ماسک ویژه اسیدی را استفاده کرد.
نحوه رقیق کردن اسید هیدروکلریک چگونه است؟
1.ابتدا اسید هیدروکلریک را در یک ظرف غیر فلزی بریزید.
2.سپس، آب را به آرامی و به تدریج به اسید اضافه کنید.
3.در حین رقیق کردن، محلول را به طور مرتب هم بزنید.
روش خنثی کردن اسید هیدروکلریک را میدانید؟
نحوه خنثی کردن اسید هیدروکلریک به صورت زیر است:
1-ابتدا اسید هیدروکلریک را با یک ماده قلیایی، مانند سدیم هیدروکسید (NaOH) یا پتاسیم هیدروکسید (KOH)، خنثی کنید.
2-سپس، محلول حاصل را با آب فراوان رقیق کنید.
نتیجه واکنش اسید هیدروکلریک با نمکهای دیگر چیست؟
اسید هیدروکلریک با نمک های دیگر واکنش می دهد و نمک جدید و اسید جدید تولید می کند. به عنوان مثال، واکنش اسید هیدروکلریک با کلرید سدیم به صورت زیر است:
اسید هیدروکلریک در چه صنایعی کاربرد دارد؟
اسید هیدروکلریک در صنایع مختلفی کاربرد دارد. برخی از این صنایع عبارتند از:
صنایع فلزی،صنایع پتروشیمی،صنایع غذایی،صنایع نساجی،صنایع کاغذ
 اسید هیدروکلریک 37% (اسید کلریدریک) (دکتر مجللی)
اسید هیدروکلریک 37% (اسید کلریدریک) (دکتر مجللی)











