با اشتراک در خبرنامه همیشه از آخرین تخفیفات و رویدادهای مهم ما مطلع خواهید شد
ارسال به سراسر کشور
تضمین کیفیت و اصالت کالا
بازگشت کالا به دلیل "انصراف از خرید" در صورتی مورد قبول است که پلمپ کالا باز نشده باشد.
معرفی بافرها
بافرها محلولهایی هستند که اگر به آنها محلول های اسیدی و یا قلیایی اضافه شود در مقابل تغییرات pH مقاومت میکنند. از بافرهای با ph مشخص ( به عنوان مثال بافر آمونیاک ) در آزمایشگاه ها و کارهای تحقیقاتی به منظور کالیبراسیون ابزار های متفاوت از جمله pH متر ها استفاده می شود.
بافر ها دارای رنج خاصی برای عملکرد صحیح خود هستند که محدوده بافری نام دارد . این محدوده برابر با یک واحد pH بیشتر و کمتر از pKa بافری است.
به طور کلی بافرها محلولهایی هستند که از مخلوط کردن یک اسید ضعیف و یک باز کونژوگه آن و یا یک باز ضعیف و اسید کونژوگه آن به دست میایند. به عنوان مثال از مخلوط کردن اسیداستیک و استات سدیم و یا هیدروکسید آمونیوم و کلرور آمونیوم بافرهای استات و آمونیوم به دست می آید.
در سیستم های زنده دو نوع سیستم بافری وجود دارد:
- سیستم بافری خارج سلولی یا پلاسما شامل بیکربنات/اسید کربنیک اسید
- سیستم بافری داخل سلولی شامل بافر فسفات او سید آمینه هیستیدین
بافر آمونیاکی، همانطور که از نامش پیداست، محلولی است که بر پایه آمونیاک ساخته شده و از آن برای ثابت نگه داشتن pH در محدوده خاصی استفاده میشود. این بافر، یک محلول آبی است که از ترکیب آمونیاک (یک باز ضعیف) و نمک آمونیوم (مانند کلرید آمونیوم) تهیه میشود.
محدوده pH: بافر آمونیاکی معمولاً pH بین 9 تا 11 را پوشش میدهد. این محدوده بستگی به غلظت آمونیاک و کلرید آمونیوم در محلول دارد.
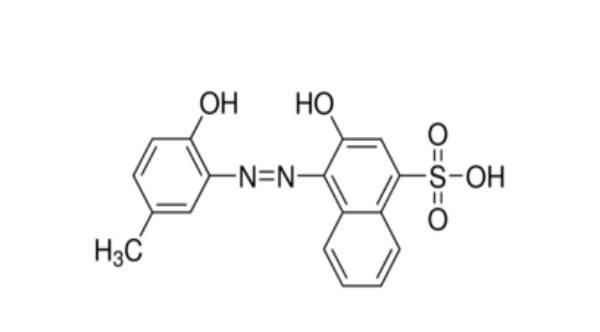
ترکیب و تهیه بافر آمونیاکی
بافر آمونیاکی که گاهی به آن بافر آمونیوم یا بافر نوترون نیز گفته میشود، یک سیستم بافری است که معمولاً از آمونیاک (NH₃) و یکی از نمکهای آن، معمولاً کلرید آمونیوم (NH₄Cl)، تشکیل میشود. این سیستم بافری برای تنظیم و حفظ pH در محدودههای خاص در محلولهای آبی استفاده میشود.
مواد مورد نیاز
- آمونیاک (NH₃) یا محلول آمونیاک
- کلرید آمونیوم (NH₄Cl)
تهیه
- یک مقدار مشخص از کلرید آمونیوم را در آب حل کنید.
- مقدار مناسبی از محلول آمونیاک به آن اضافه کنید تا به pH مورد نظر برسید.
چرا از بافر آمونیاکی استفاده میکنیم؟
- ثابت نگه داشتن pH:
بافرها در برابر تغییرات pH مقاومت میکنند و به همین دلیل در بسیاری از آزمایشها و فرآیندهای صنعتی که به pH مشخصی نیاز دارند، کاربرد دارند. - تنظیم pH:
میتوان با تغییر نسبت آمونیاک به نمک آمونیوم، pH بافر را تنظیم کرد. - کاربرد در صنایع مختلف:
از بافر آمونیاکی در صنایع غذایی، دارویی، شیمیایی، و آزمایشگاهی استفاده میشود.
جدول مشخصات فیزیکی و شیمیایی تقریبی بافر آمونیاکی 10
| مشخصه | مقدار تقریبی | واحد | توضیحات |
|---|---|---|---|
| ظاهر | مایع شفاف و بیرنگ | - |
|
| بو | بوی تند و مشخص آمونیاک | - |
|
| pH | حدود 9.25 | - | بسته به نسبت آمونیاک به نمک آمونیوم متغیر است |
| چگالی | حدود 0.96 گرم بر سانتیمتر مکعب | g/cm³ |
|
| نقطه جوش | حدود 100 درجه سانتیگراد | °C | بسته به فشار محیط متغیر است |
| نقطه انجماد | زیر 0 درجه سانتیگراد | °C |
|
| حلالیت در آب | به هر نسبت با آب مخلوط میشود | - |
|
| هدایت الکتریکی | هادی متوسط جریان برق | - |
|
| پایداری شیمیایی | در شرایط معمولی پایدار است، اما در مجاورت اسیدها تجزیه میشود | - |
|
| خطرناک بودن | ماده خورنده و سمی است. تماس با پوست، چشم و دستگاه تنفسی میتواند باعث آسیب شود. | - |
|
توجه: این جدول تنها یک نمای کلی از خواص بافر آمونیاکی ارائه میدهد. برای اطلاعات دقیقتر و ایمنی، همیشه به برگه اطلاعات ایمنی (SDS) محصول مراجعه کنید.
- محلول در آب: بافر آمونیاکی به راحتی در آب حل میشود.
- قلیایی: به دلیل وجود آمونیاک، بافر آمونیاکی خاصیت قلیایی دارد.
- قابلیت تنظیم pH: با تغییر نسبت آمونیاک به نمک آمونیوم، میتوان pH بافر را در محدوده وسیعی تنظیم کرد.
مکانیسم عملکرد تنظیم pH
هنگامی که یک اسید به بافر آمونیاکی اضافه میشود، آمونیاک موجود در بافر با آن واکنش داده و یون آمونیوم تشکیل میدهد. این واکنش باعث میشود که تغییرات pH به حداقل برسد. برعکس، هنگامی که یک باز به بافر اضافه میشود، یون آمونیوم با آن واکنش داده و آمونیاک آزاد میکند. این واکنش نیز باعث ثابت ماندن pH میشود.
کاربردهای بافر آمونیاکی
- تعیین ثابت تفکیک اسیدها و بازها: با استفاده از بافر آمونیاکی میتوان ثابت تفکیک اسیدها و بازهای ضعیف را تعیین کرد.
- کالیبراسیون دستگاه پی اچ متر (pH متر): بافر آمونیاکی به عنوان یکی از استانداردهای کالیبراسیون pH متر استفاده میشود.
- تثبیت pH در واکنشهای شیمیایی: در بسیاری از واکنشهای شیمیایی و برای فعالیت صحیح آنزیم ها که نیاز به pH مشخصی دارند، از بافر آمونیاکی استفاده میشود.
- صنایع غذایی: در برخی فرآیندهای تولید مواد غذایی برای تنظیم pH استفاده میشود.
- حمل نمونه های زیستی
- ساخت فرآورده های بهداشتی چون انواع شامپو و مواد آرایشی
- صنایع الکل سازی و رنگ سازی
نکات ایمنی و ذخیرهسازی بافر آمونیاکی
بافر آمونیاکی یک محلول شیمیایی است که به دلیل خواص قلیایی و بخارات سمی آمونیاک، نیازمند رعایت نکات ایمنی خاصی است. در ادامه به برخی از مهمترین نکات ایمنی و ذخیرهسازی این محلول اشاره میشود:
نکات ایمنی حین کار با بافر آمونیاکی
- دستکش: همیشه از دستکشهای مقاوم در برابر مواد شیمیایی استفاده کنید.
- عینک ایمنی: برای محافظت از چشمها در برابر پاشش محلول از عینک ایمنی استفاده کنید.
- ماسک: در محیطهایی با تهویه نامناسب، از ماسکهای تنفسی مناسب برای جلوگیری از استنشاق بخارات آمونیاک استفاده کنید.
- لباس محافظ: از لباسهای محافظ مانند روپوش آزمایشگاهی استفاده کنید.
- تهویه مناسب: محیط کار با بافر آمونیاکی باید دارای تهویه مناسب باشد تا از تجمع بخارات آمونیاک جلوگیری شود.
- دور از منابع حرارت: بافر آمونیاکی را دور از منابع حرارت، جرقه و شعله نگهداری کنید.
- جلوگیری از تماس با پوست، چشم و دستگاه تنفسی: در صورت تماس با پوست، چشم یا استنشاق بخارات آمونیاک، بلافاصله ناحیه آلوده را با آب فراوان شستشو داده و به پزشک مراجعه کنید.
- دور از مواد ناسازگار: بافر آمونیاکی را دور از اسیدها، اکسید کنندهها و فلزات سنگین نگهداری کنید.
ذخیرهسازی بافر آمونیاکی
- ظروف مقاوم: بافر آمونیاکی را در ظروف مقاوم در برابر مواد شیمیایی، محکم بسته و در مکانی خنک، خشک و دور از نور مستقیم خورشید نگهداری کنید.
- برچسبگذاری: ظروف حاوی بافر آمونیاکی را به روشنی برچسبگذاری کرده و اطلاعات مربوط به ماده شیمیایی، تاریخ تولید و تاریخ انقضا را روی آن درج کنید.
- جدا از مواد دیگر: بافر آمونیاکی را جدا از مواد دیگر، به ویژه مواد قابل احتراق و اکسید کنندهها نگهداری کنید.
- محل نگهداری قفل شده: محل نگهداری بافر آمونیاکی باید قفل شده و دور از دسترس کودکان و افراد غیرمجاز باشد.
شرایط نگهداری بافر آمونیاکی
- اگر محلول بافر خود را به صورت شرکتی تهیه کرده اید، ظرف طراحی شده توسط خود شرکت ایده آل ترین ظرف برای نگهداری محلول بافر مورد نظر خواهد بود.
- حتما از بسته بودن درب محلول مطمئن شده و به تاریخ انقضای درج شده روی آن نیز توجه کنید. محلول های بافری طول عمر مشخصی دارند و بعد از آن به تدریج قدرت بافری خود را از دست می دهند.
- جهت نگهداری هر چه بهتر محلول های بافری بهتر است آن ها را در دمای محیط نگهداری کنید. افزایش بیش از حد دما یا سرد بودن محیط نگهداری بافر می تواند روی خواص و کارکرد آن تاثیر زیادی بگذارد.
- محلول های بافر باید دارای مشخصات حجمی تادورقم اعشار، جدول تغییارات PH با دما و تاریخ باز شدن درب ظروف باشند.
- درصورت مشاهده هرگونه تغییرات فیزیکی (رسوب ، کدورت و … ) ازمصرف محلولها خودداری شود.
فروش بافر آمونیاکی
بافر آمونیاکی یک ابزار ارزشمند در آزمایشگاهها و صنایع است که برای کنترل و ثابت نگه داشتن pH در محدوده مشخصی استفاده میشود. با درک مکانیسم عملکرد و ویژگیهای این بافر، میتوان از آن به طور موثر در آزمایشها و فرآیندهای مختلف استفاده کرد.
"ای آز" فروشگاهی فعال در حوزه فروش اینترنتی مواد شیمیایی صنعتی و آزمایشگاهی و تجهیزات آزمایشگاهی-پژوهشی است که آماده فروش بافر آمونیاکی در بسته بندی های مقرون به صرفه و با کیفیت ممتاز در گریدهای صنعتی و آزمایشگاهی و از برندهای معتبر ایرانی، هندی، چینی و اروپایی به پژوهشگران، دانشگاهیان، صنایع و کارخانجات است.

خرید بافر آمونیاکی
چگونه میتوان pH بافر آمونیاکی را تغییر داد؟
با تغییر نسبت آمونیاک به نمک آمونیوم میتوان pH بافر را تنظیم کرد. افزایش نسبت آمونیاک pH را افزایش داده و افزایش نسبت نمک آمونیوم pH را کاهش میدهد.
آیا بافر آمونیاکی سمی است؟
بله، آمونیاک یک ماده سمی است و تماس با آن میتواند باعث تحریک پوست، چشم و دستگاه تنفسی شود.
تفاوت بافر آمونیاکی با سایر بافرها چیست؟
بافر آمونیاکی یک بافر قلیایی است و pH آن معمولاً در محدوده قلیایی قرار دارد. سایر بافرها مانند بافر فسفات، بافر استات و ... ممکن است pH متفاوتی داشته باشند و برای کاربردهای خاصی مناسبتر باشند.
آیا بافر آمونیاکی با دیگر حلالها قابل مخلوط کردن است؟
بله، بافر آمونیاکی با بسیاری از حلالهای آلی دیگر مانند متانول و اتانول قابل مخلوط کردن است و میتواند به عنوان حلال مخلوط استفاده شود.
چگونه میتوان نشت بافر آمونیاکی را مدیریت کرد؟
در صورت نشت، محل را با مواد جاذب مانند کاغذ جاذب یا خاک اره پاک کرده و مواد جاذب آلوده را در ظرف مناسب قرار دهید.
آیا بافر آمونیاکی در آزمایشگاههای تحقیقاتی استفاده میشود؟
بله، به دلیل خلوص و پایداری pH بالا، این بافر به طور گسترده در آزمایشگاههای تحقیقاتی استفاده میشود.
 بافر آمونیاکی (نوترون)
بافر آمونیاکی (نوترون)